復必泰二價疫苗於香港自費接種服務正式開始 為有需要人士提供更多疫苗選擇
(2023年1月6日,中國香港)-上海復星醫藥(集團)股份有限公司(「復星醫藥」或「集團」,股票代碼:600196.SH,02196.HK)宣佈,自2023年1月6日起,復星醫藥開始為中國香港地區的私營醫療體系供應復必泰二價疫苗,有需要人士可在提供復必泰二價疫苗的診所或醫療機構進行自費接種。
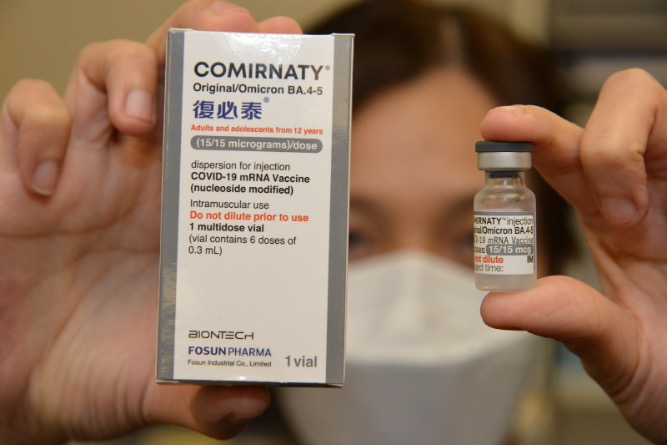
圖1:復必泰二價疫苗

圖2:2023年1月6日,復必泰二價疫苗於香港自費接種服務正式開始
2022年12月,復必泰二價疫苗獲香港衛生署正式註冊為藥品/製品(生物製品),用於12歲及以上人群的加强接種。復必泰二價疫苗是已上市復必泰BNT162b2的迭代和補充,可有效應對Omicron變異株。復必泰二價疫苗每劑含有15微克編碼原始毒株刺突蛋白的mRNA和15微克編碼Omicron BA.4/BA.5變異毒株刺突蛋白的mRNA。
根據正在進行的2/3期全球臨床試驗顯示,以復必泰二價疫苗作加强劑接種1個月後,可產生强烈的中和抗體反應,與接種加强劑前相比,55歲以上人士的中和抗體可提高13.2倍,而18-55歲人士的中和抗體則提高9.5倍。這表明復必泰二價疫苗加强劑或較原始株疫苗對Omicron BA.4/BA.5變種病毒產生更高的保護。
此外,針對當前在中國香港地區及眾多亞洲國家和地區肆虐的Omicron BA.4/BA.5亞系變種病毒(包括BA.4.6, BA.2.75.2, BQ.1.1及XBB.1),復必泰二價疫苗相對原始株疫苗產生更高免疫反應,兩種疫苗的安全性及耐受性相若。一項針對復必泰二價疫苗對Omicron新亞系變種病毒所產生的抗體反應分析研究顯示,接種復必泰二價疫苗後,針對BQ.1.1和XBB.1的中和抗體滴度可分別提高8.7倍和4.8倍。
隨著內地與香港逐步有序全面恢復往來,赴港接種復必泰疫苗將成為民眾防疫新選擇。2023年1月6日,復星健康平台正式開啟復必泰二價疫苗赴港接種預約,同時復星健康也與京東健康、美團、阿里健康、百度健康、微醫、春雨醫生等平台陸續開展合作,有需求的用戶可通過上述任一平台進行線上預約,預約成功後即可赴港自費接種復必泰二價疫苗。復星健康作為復必泰疫苗內地首個履約服務平台,已與香港多家醫療機構及診所達成戰略合作關係,將為內地居民赴港接種復必泰疫苗提供一站式便捷服務。
未來,復星醫藥將一如既往,積極配合香港特區政府的疫苗接種計劃安排,持續為香港提供穩定的疫苗供應,切實協助香港應對疫情。同時,復星醫藥也將穩妥有序地推進私營市場新冠疫苗的供應及服務,為有需要的人士提供更多疫苗選擇。
***
關於復星醫藥
上海復星醫藥(集團)股份有限公司(「復星醫藥」,股票代碼:600196.SH,02196.HK)成立於1994年,是一家植根中國、創新驅動的全球化醫藥健康產業集團,直接運營的業務包括製藥、醫療器械、醫學診斷、醫療健康服務,並通過參股國藥控股覆蓋到醫藥商業領域。
復星醫藥以患者為中心、臨床需求為導向,通過自主研發、合作開發、許可引進、深度孵化等多元化、多層次的合作模式,豐富創新產品管線。圍繞腫瘤及免疫調節、代謝及消化系統、中樞神經系統等重點疾病領域,復星醫藥已搭建和形成了小分子創新藥、抗體藥物、細胞治療技術平台,並積極探索RNA、基因治療、ADC、靶向蛋白降解等前沿技術領域,提升創新能力。
在「4IN」(創新Innovation、國際化Internationalization、智能化Intelligentization、整合Integration)戰略的指導下,復星醫藥將秉承「創新轉型、整合運營、穩健增長」的發展模式以及為股東創造價值的信念,不斷加强自主研發與外部合作,豐富產品管線,强化全球化佈局,提升運營效率。同時,積極推進醫療健康產業線上線下佈局,致力於成為全球醫療健康市場的一流企業。
瞭解公司更多資訊可登錄官網:www.fosunpharma.com。
復星醫藥前瞻性聲明
本新聞稿包含復星醫藥的前瞻性聲明。這些前瞻性聲明內容可能包括但不限於:復星醫藥抗擊新冠疫情的努力;復星醫藥與BioNTech之間為研發潜在的新冠疫苗而開展的合作;復星醫藥基於最新的觀測資料對新冠疫苗在臨床試驗和/或商業應用中的潜在特性作出的預期;臨床資料的性質(須接受持續的同行評審、監管審查和市場判讀);提交上市許可或緊急使用授權相關資料或收到上市許可或緊急使用授權的時間;復星醫藥計畫的運輸和儲存方案;以及獲批後,BioNTech與復星醫藥供應新冠疫苗滿足市場需求的能力,包括復星醫藥對2022年產量的估計。本新聞稿中的前瞻性聲明均基於復星醫藥目前對未來事件的預期和信念,但由於存在若干風險和不確定性,實際結果可能與這些前瞻性聲明所陳述或暗示的結果存在重大和不利的差异。這些風險和不確定性包括但不限於:研發過程中固有的不確定性(包括滿足臨床試驗預定終點、臨床試驗開始和/或完成日期、監管資料提交日期、監管批准日期和/或上市日期的能力)以及臨床資料相關的風險,包括出現新的不利臨床試驗資料的可能性和對現有臨床試驗資料的進一步分析;得出類似臨床結果或其他結果的能力,包括復星醫藥聲明之後在臨床試驗剩餘部分或商業化後在更大、更多樣化人群中觀察到的疫苗有效率、安全性和耐受性情况;疫苗更廣泛使用後,出現有關有效性、安全性或其他開發方面的新資訊的風險,包括額外不良反應的風險,其中一些不良反應甚至可能是嚴重的;是否以及何時可以在特定司法管轄區提交新冠疫苗許可和/或緊急使用授權申請;關於新冠疫苗的未决申請或已提交的申請,是否以及何時可能獲得特定監管機構的批准(取决於諸多因素,包括疫苗的獲益是否超過其已知風險、疫苗有效性等);是否能及時滿足特定監管機構針對有條件批准提出的條件;生產設施是否以及何時可以獲得特定監管機構的認證或確認;復星醫藥與合作夥伴或協力廠商供應商之間的關係中斷;疫苗生產原料供應相關的風險; BioNTech的生產能力是否能滿足復星醫藥的疫苗需求;生產穩定性中斷;復星醫藥疫苗超低溫運輸和儲存方面的挑戰;是否以及何時達成額外的供應協議以及其他潜在困難等。
本新聞稿中包含的資訊截至2023年1月6日。復星醫藥無義務根據任何新資訊、未來事件或研發進展更新本新聞稿中的前瞻性聲明。
關於風險和不確定性的詳細資訊,可參見復星醫藥截至2021年12月31日止財政年度的年度報告,及截至2022年6月30日止財政年度的中期報告(包括「潜在風險」章節),這些報告均已提交香港聯合交易所和上海證券交易所備案,可登陸www.hkexnews.hk、www.sse.com.cn和www.fosunpharma.com查閱。





