创新引领!复星医药荣登2026全球药企研发管线规模TOP 20



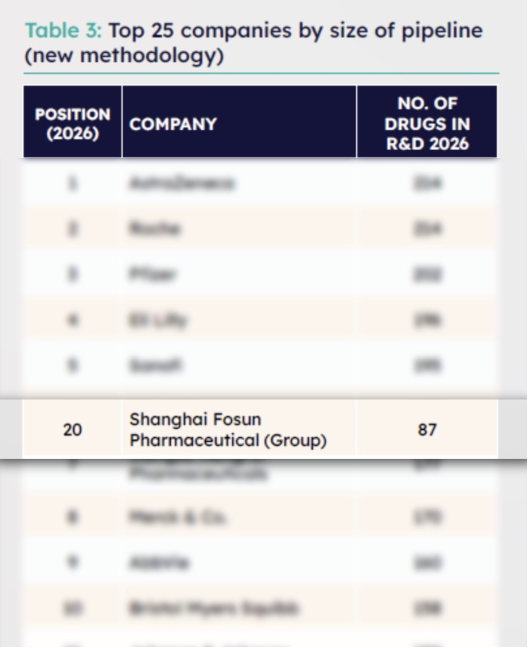
近日,全球知名咨询机构Citeline发布《2026年医药研发年度回顾》白皮书(Pharma R&D Annual Review 2026),评选出全球管线规模排名前25的制药公司。根据本年度最新的统计方法,复星医药成功入选该榜单,位列第20位。
为了更精准的展现全球药企的活跃管线数量,今年开始,排名统计将采用全新的统计方法,着重展现企业当前仍在推进的活跃管线数量,以此真实反映企业的研发活跃度与未来发展潜力。复星医药入选该国际权威榜单,标志着公司创新研发实力与管线质量获得国际专业认可。
深耕核心治疗领域,构建差异化临床管线
作为一家创新驱动的全球化医药健康产业集团,复星医药已形成开放式、全球化的创新研发体系,围绕未满足临床需求,深度布局肿瘤、免疫炎症、神经退行性疾病等核心治疗领域,积极拓展慢病及罕见病等领域,打造具有长期竞争力的产品管线与综合解決方案。同时,复星医药持续夯实抗体/ADC、小分子、细胞治疗等核心技术平台,拓展核药、小核酸等前沿技术,强化早期创新能力,加速科研成果转化。
2025年,复星医药全年研发总投入共计59.13亿元,同比增长6.46%,其中,创新药品相关研发投入达43.03亿元、同比增长15.98%,占制药业务研发投入的80.26%。2025年复星医药共有7个创新药品共16项适应症于境内外获批上市,6个创新药品种的上市申请获受理,近40项创新药临床试验获中美欧批准,多个核心产品进入关键临床阶段,为后续商业化增长奠定了坚实的管线基础。
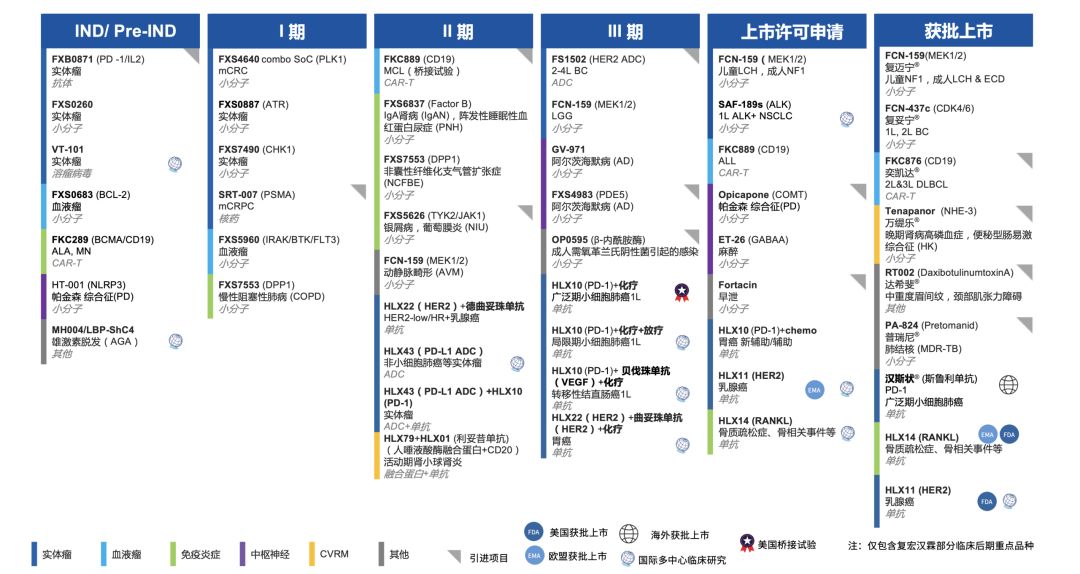
在肿瘤领域,自研小分子创新药复迈宁(芦沃美替尼片)双适应症国内获批,填补国内罕见肿瘤治疗空白;CDK4/6抑制剂复妥宁(枸橼酸伏维西利胶囊)2项适应症上市,为乳腺癌患者带来全新治疗选择。抗PD-1单抗斯鲁利单抗注射液在欧洲及多个新兴市场获批,成为全球首个在欧盟获批用于一线治疗广泛期小细胞肺癌的抗PD-1单抗,截至2025年末,斯鲁利单抗注射液累计已在全球超过40个国家和地区获批上市,联合化疗一线治疗ES-SCLC的美国桥接试验已完成患者入组,计划2026年向FDA递交相应生物制品许可申请(BLA)。HLX43、HLX22等抗体/ADC药物已进入关键临床阶段,第二款CAR-T产品布瑞基奥仑赛的上市申请也已获受理。2026年3月31日,复星医药宣布与梯瓦合作开发的肿瘤免疫治疗创新疗法FXB0871在中国获批开展I期临床,将加速这一全球前沿创新疗法落地中国,让患者尽早受益于全球领先的创新疗法。
在免疫炎症与慢病领域,许可引进的First-in-Class创新药万缇乐(盐酸替那帕诺片)获批上市,为中国慢性肾脏病透析患者提供全新治疗方案;FXS7553等核心产品临床进展稳步推进。
在神经退行性疾病领域,帕金森病治疗药物奥吡卡朋胶囊通过“先行先试”政策在海南博鳌落地;甘露特钠胶囊纳入阿尔茨海默病创新药管线,并推进上市后确证性临床试验;许可引进的AR1001已进入全球多中心III期临床。
此外,复星医药前瞻性布局核药、小核酸等前沿赛道,核药项目SRT-007顺利启动I期临床试验,初步建立“影像诊断 - 靶向治疗”的诊疗一体化研发路径;细胞治疗领域自体双靶点CAR-T产品FKC289临床试验申请获国家药监局受理,为后续创新产品储备持续赋能。
展望未来,复星医药将继续以患者为中心,围绕未被满足的临床需求,持续加大创新投入,高效推进全球领先技术和创新产品的研发与转化落地。同时,以全球视野整合创新资源,以数字智能驱动运营升级,致力于成为全球领先的医疗创新整合者,为全球患者提供更多优质、可及的医疗健康解决方案。
联系方式

媒体:pr@fosunpharma.com
投资人:ir@fosunpharma.com










